バイオシミラーの医薬品リスク管理計画(RMP)とその実施結果について
医薬品リスク管理計画(Risk Management Plan;以下、RMP)は医薬品のリスク(副作用)を最小化し、安全性を確保するために、開発の段階から市販後までの一連のリスク管理を計画書としてまとめたものです。医薬品の製造販売業者はRMPに則り、安全性を監視し、リスクを低減するための取組みを行い、定期的な評価を実施していきます(図1参照)。
| 重要な特定されたリスク | 医薬品との関連性が十分な根拠に基づいて示されている有害な事象のうち重要なもの |
|---|---|
| 重要な潜在的リスク | 医薬品との関連性が疑われる要因はあるが臨床データ等からの確認が十分でない有害な事象のうち重要なもの |
| 重要な不足情報 | 治験から除外されていた対象患者集団等で医薬品リスク管理計画を策定した時点では十分な情報が得られておらず、安全性を予測する上で不足している情報のうち重要なもの |
平成24年4月11日付 薬食安発0411第1号・薬食審査発0411第2号「医薬品リスク管理計画指針について」より抜粋して引用
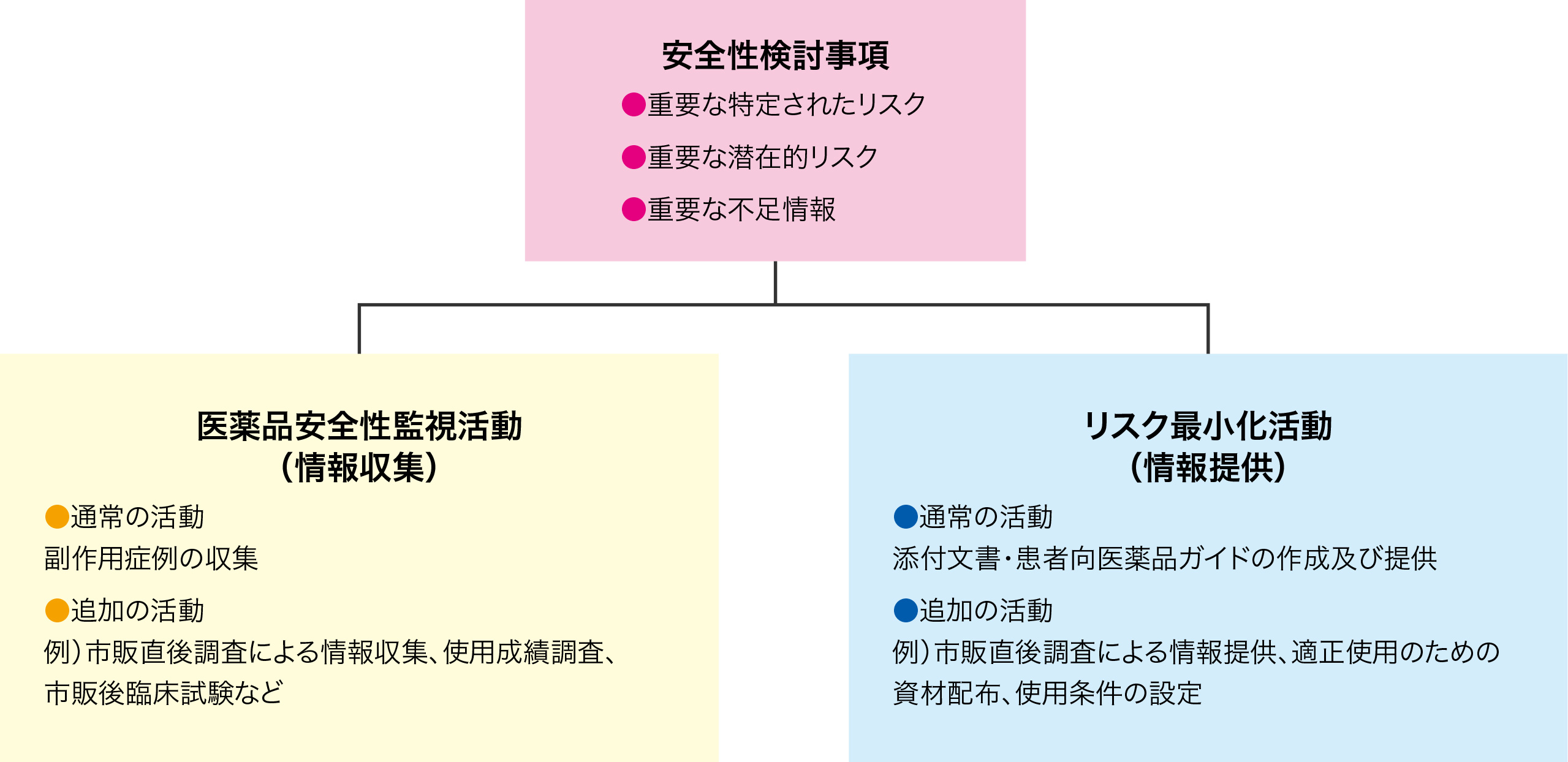
RMPでは開発から市販後に至って得られた情報から「安全性検討事項」として3種類のリスクを設定しています(表1参照)。
そして、この安全性検討事項に対し、「医薬品安全性監視活動(情報収集活動)」と「リスク最小化活動(情報提供活動)」をどのように行うかを計画しています。なお、各活動は全医薬品共通して行われる活動(通常の活動)と医薬品の特性に合わせて行われる活動(追加の活動)があります。
また、「医薬品安全性監視活動」の追加の活動の一つとして製造販売後調査を実施することがあります(表2参照)。必ず実施するものではなく、承認前の治験等から得られる情報、発売後に医療機関等から得られる情報を元に必要に応じて実施されます。2018年からは新たな製造販売後調査の手法として製造販売後データベース調査が追加され、近年バイオシミラーでも多く実施されています。
| 使用成績調査 | 医療機関から収取した情報を用いて、診療において、医薬品の副作用による疾病等の種類別の発現状況並びに品質、有効性及び安全性に関する情報の検出又は確認のために行う調査 |
|---|---|
| 製造販売後データベース調査 (2018年~) |
医療情報データベースを用い、医薬品の副作用による疾病等の種類別の発現状況並びに品質、有効性及び安全性に関する情報の検出又は確認のために行う調査 |
| 製造販売後臨床試験 | 治験、使用成績調査、製造販売後データベース調査の成績に関する検討を行った結果、得られた推定等を検証し、又は診療においては得られない情報を収集するため、承認された用法、用量、効能・効果に従い行う試験 |
令和5年9月20日付 厚生労働省 第13回 医薬品等行政評価・監視委員会
資料2-1「医薬品の製造販売後調査(使用成績調査20等21年4月1日)について」より抜粋して引用
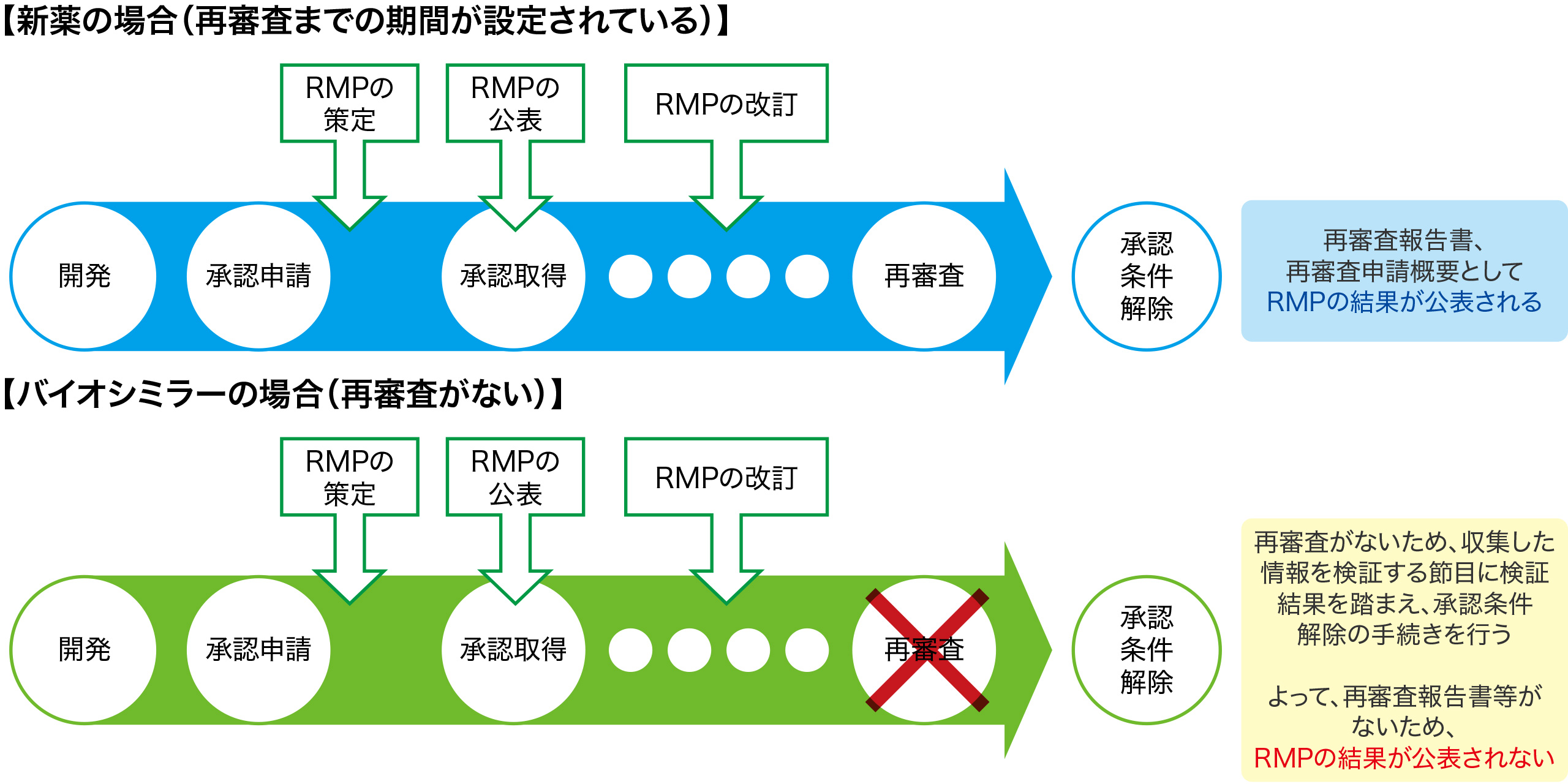
バイオシミラーは新医薬品と共に平成25年4月1日以降に製造販売承認申請を行う品目からRMPの策定が求められることになり1)、承認条件として「医薬品リスク管理計画を策定の上、適切に実施すること」が付与されています。上述の通り、「医薬品安全性監視活動」の追加の活動として製造販売後調査を実施するバイオシミラーも多く、通常はこの調査終了後に承認条件解除の手続きが行われます。
しかしながら、バイオシミラーの承認条件が解除された際は新医薬品とは異なり、RMPの実施結果が公表される機会はありません(図2参照)。そこで、RMPが適切に実施され、承認条件が解除されたバイオシミラーの「RMP実施結果の概要」を弊協議会ホームページに掲載し、情報発信を行うことにしました(表3参照)。
バイオシミラー協議会作成
*製造販売後データベース調査
- 1)平成24年4月11日付 薬食安発0411第1号・薬食審査発0411第2号「医薬品リスク管理計画指針について」
「RMP実施結果概要」のformat作成においては、RMPの通常の活動は先行バイオ医薬品とバイオシミラーは同じであるため、RMPの追加の活動をメインに情報提供することとしました。なお、format作成には、日本製薬工業協会 医薬品評価委員会PV部会にもご協力をいただきました。
掲載をご希望される際は、当協議会の定めたformatで「RMP実施結果概要」を作成し、JBSA事務局(info@biosimilar.jp)に電子メールで送ってください。電子メールのタイトルは【RMP実施結果概要掲載依頼】としてください。
バイオシミラーに関する通知等は「独立行政法人 医薬品医療機器総合機構(PMDA)の承認審査関連業務-バイオ後続品」のページをご覧ください。